���F�ڵ�λ�ã� �ٝ�����ˎ���W��� >> �[���� >> �о��Mչ
������ӆ���ΰ��ֲ������ί�Ҏ�����ҹ��R��
- ��Դ�� �Ї��t�WՓ���� ���ߣ����ɽ��� �l���r�g��2011-6-22 3:40:00
���x���ֲ������ί��ǽ���Ӱ���g���������[���M�а���λ���������W�ķ��������[���M�����ί���Ӱ���������g��������CT�ʹŹ������MRI�������ί�;��������Ƥ������ǻ�R���g�ͽ��_�����g���N�������ƄӸΰ��ֲ������ί���Ҏ������CSLC��CSCO�����A�t�W���β��W�֕��ΰ��W�M��ͬ�l�𣬽M����ơ��[������������ȶ����W�ƵČ��҅��c�������ӆ�ˡ��ΰ��ֲ������ί�Ҏ�����ҹ��R������������ӑՓ��
�����ֲ������ί������c������ֱ���������[�������и�Ч���ٵă��ݣ��ί������������[�������܇��M�������C�wӰ�С�����Է��͑��á��ֲ������ί����^ȥ��20�����ҰlչѸ�ͣ��ѽ��ɞ��^���g�г��������ί���ĵ�3��ΰ��ί��ֶΣ����������䯟Ч�_�У��e����С�ΰ����ί����棬���l���گ�Ч�c���g�г��������˱��J����С�ΰ��ĸ������ί��ֶ�֮һ��
�����ί�ԭ�������
�����ֲ������ί�����ԭ���ɷ֞黯�W�����ί������������ί������W������ָ�û��W�ķ��������������ע�뻯�W���|��oˮ�ƾ�������ȣ���ʹ�ֲ��M������Óˮ�����������⣬�Ķ��_������[�������Ŀ�ġ�Ŀǰ�����ڸΰ��ί��Ļ��W���ڷ�����Ҫ�����ȟoˮ�ƾ�ע�䣨PercutaneousEthanol Injection��PEI�������ȟoˮ����ע�䣨Percutaneous Acetic AcidInjection��PAI���ȡ�
�����������ڄt��ͨ�^�ӟ������ֲ��M�������[��������ί���������Ҫ�����l�����g��Radiofrequency Ablation��RFA�������̻��g��Microwave Coagulation Therapy��MCT��������ί���Cryoablation�����۽������ڣ�High Intensive Focused Ultrasound��HIFU�������������ί��ȡ�
������Ҏ�����²��������l�����g��������m�������̻��g�����ɹ������ֲ������ί�����������
�����ί�ԭ�t
����1.���l�ί�ǰ횳���u�����߲��鼰���[������W�О飨�A�y�����Լ�Ч�����_�������ί������ί��Ĵ�ʩ�����E����
����2.�ί�ǰ�г��Ӱ��W�u���������[������������λ�õ��ƶ��ί����������ԣ����C���İ�ȫ�������M���ܫ@��һ���ԡ��m�ε���ȫ�����ί���
����3.�x���m�ϵ�Ӱ������·�������O���ί��^�̡�
����4.�ƶ��m�˵ľC���ί��������ƌW�������S�LӋ����
��
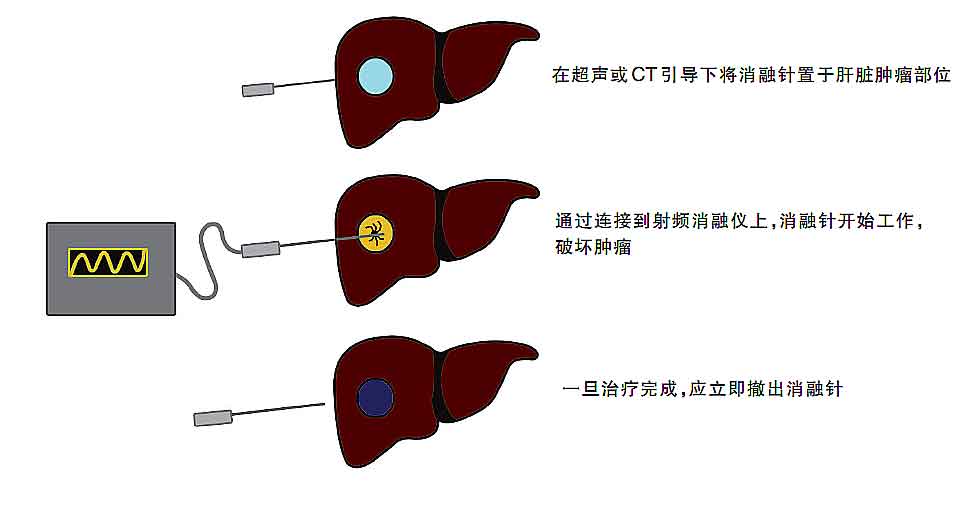
�m���C�ͽ����C
�����m���C
����1.�ΰl�[�������ֱ��≤5 cm�������[����Ŀ≤3�������ֱ��≤3 cm��
����2.�]���}�ܰ�˨�����������ַ���
����3.�ι��ּܷ���Child-Pugh A��B���ȿ��ί��_��ԓ�˜ʡ�
����4.�������g�г���ֱ����5 cm�Ćΰl�[�������ֱ����3 cm�Ķ�l�[�����ֲ����ڿ������Ϣ���ί������ί���һ���֡�
���������C
����1.�[�����ߏ����ΰ���
����2.�����}�ܰ�˨�������������ַ���
����3.�ι��ּܷ���Child-Pugh C�����o���ί��o�����ơ�
����4.�ί�ǰ1 ������ʳ�ܣ�θ�ף��o�}�������ѳ�Ѫ��
����5.���ɼm������Ѫ�����ϵK������Ѫ�����Ї��س�Ѫ�A��
����6.�B���Դ�����ˮ����Һ�|��
����7.����Ը�Ⱦ��������đ��ϵ�y�װY�ȡ�
����8.���صĸΡ��I���ġ��Ρ��X����Ҫ�K������˥�ߡ�
����9.�������R�ϵK��������ί���
�������⣬��һ���T�^�[�������������C���[���o�Nđ�ҡ�θ�c��������ͻ���ڸΰ�Ĥ�齛Ƥ����·�������������C�����и����D�ƵIJ������ҕ����ɣ���Ȼ���Բ��þֲ������ί����ƸȲ�����r��
�����gǰ�ʂ�
����1.�ί�ǰ���ƙz�飺Ѫ��Ҏ��������Ҏ����Ѫ���ܡ��[����־���늈D����Ƭ�����z�飬��Ҫ�r�M���ķι��ܙz�顣
����2.���ó����Зl���߱M���x����Ӱ�z�飩��������CT/MRI �șz���u�r�[����r�����x�������������ʽ�������ί��x����
����3.���_�\�࣬��Ҫ�r�д��̻�z���\���˜ʅ����Ї������f���ΰ����Iί�T��2001���ƶ����\���˜ʣ���
����4.���g�^�ʹ��̲�λ��Ƥ��
����5.���ڃx���Ĝʂ䣺�ί�ǰ�șz�������ί��x���Ƿ�̎�ڹ�����B���ܷ�����������늘O��·�Ƿ�ʂ�õȡ�
����6.�������g֪��ͬ��������g�ί�ǰÿλ���ߺ���֪��ͬ�������֪���g�^�̡��L�U���A����ܣ����֪��ͬ�⡣
����������
�����ΰ��ֲ������ί����Խ�Ƥ������ǻ�R���_���g���M�С�
������Ƥ�ΰ��ֲ������ί�������CT������
����1.�gǰ��ʳ8 С�r����Ԕ�����z�飨����xCTƬ�������_���K������r���ƶ��������M�·���Ͳ�ᘷ�����
����2.����������ҕ��r�x���c�ֲ��������o�}�ʹ���o�}������ӲĤ�������͚���������ʹ������ʽ��
����3.���g�^��Ҏ������䁽���
����4.�M���ٴ�ȫ�泬��CT����z�飬�_���M��c���MᘽǶȺͲ���Լ���ᘷ������M���x���Ƚ��^�����������K�����M���[����
����5.�M���x�����g�Mᘣ��ڳ�/CT�����£��M���x���Ƚ��^�����������K�����M���[�������̑��ʴ_��λ�����ⷴ�Ͷ�δ��̣������[���Nֲ���p�������M�����[�����ѳ�Ѫ�ȣ�����M��^�����ֱ�ӌ�늘O��˻أ����Ǒ�ԓ��ԭλ���ں���������¶�λ�������[���Nֲ��һ����r�£����������^�λ���[�����������^�\��λ���[����
����6.���ո������ί��x���f�����M�������ί������c�M�С���_�������ί���Ч�������ڷ�����ԓ�����_��0.5 cm �İ�ȫ߅�磬һᘶ��c���دB���ڷ�ʽ���Ա��C���ڷ����͜p��©�յİl����������ɺ�ȡ�ړ�ᘕr�M��ᘵ����ڣ���ֹ�g���Ѫ���[����ᘵ��Nֲ��
����7.�ί��Y��ǰ�M���ٴγ�/CT��ȫ�������K���_�����ڷ����ѽ���ȫ���w�[����������0.5��1.0 cm�İ�ȫ����߅�磬���ų��[�����ѡ���Ѫ����Ѫ�����صȲ��l�Y�Ŀ��ܡ�
��������ǻ�R�ֲ������ί����m�����[��λ�ڸΰ�Ĥ�£���������đ�ҡ�θ�c�ȣ����߳�/CT �@ʾ������y�ڽ�Ƥ�����ߣ�
������Ҏ��ǻ�R��������Ҫ�r���x�����g�����M������¶���K���[������Ҫ�r�����ø�ǻ�R������_���[����Ŀ����λ�����x�����x���o�܇������M�����٣������lᘽ�Ƥ�����븹�����ڸ�ǻ�Rֱҕ�»��߸�ǻ�R��������늘Oᘲ����[���ȣ����A��������ᘣ��������ί��������^���пɣ�����ֹѪ�Q����е���g�ࡢ����������KѪ�������������Ч�ʣ��������ڷ�����������ɺ��м��z�飬�_���o����Գ�Ѫ���������ٓp����
�����_���ֲ������ί����m���������ɷN�����y�ڌ��У��������g̽��l�F�[���o���г��ߣ�
��Ҏ�_�������x�����g������¶�[�������o�܇������M�����٣��g�г�������늘Oᘲ����[���ȣ����A��������ᘣ������ί��������^���п��g�ࡢ����������KѪ�������������Ч�ʣ��������ڷ�����������ɺ��м��z�飬�_���o����Գ�Ѫ���������ٓp�����P����
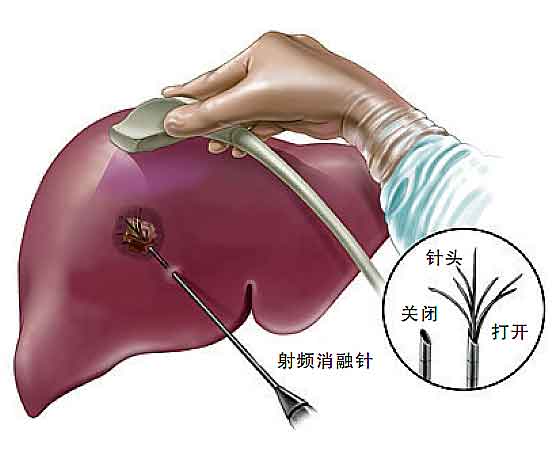
���l�����M��������ᘵIJ���ʾ��
�g��ע�����
�����g��Ҏ��ʳ���O�y�����w��4С�r���P��6С�r���ϣ�ע��O�yѪ��Ҏ�����I���ܵȣ����o���o�Ρ��A����Ⱦ���ʹ��ֹѪ��̎�����A�����l�Y�İl�����l�����l�Y���M�зe�O̎����
�������l�Y���A����̎��
�������l�Y�ķּ�
�����ֲ����ڲ��l�Y�ɷ֞��p�Ȳ��l�Y���ضȲ��l�Y��
�����p�Ȳ��l�Y��minor complication��
����A�����o���ί����o���������B���������S�ί����o��������������H��һҹ���^�졣
�����ضȲ��l�Y��major complication��
����C������Ҫ�ί���סԺ�r�g���L��48С�r��
����D������Ҫ�����ί����������t�o���e��
����סԺ�r�g���L��48С�r��
����E�����������L�õĺ��z�Y��
����F����������
�������īI��������l���ھ��кܸߵİ�ȫ�ԡ��īI����������ʞ�0��1%�����l�Y�l���ʞ�0��12%�����У��p���l�Y�İl���ʼs��4.7%����Ҫ�аl�ᡢ��ʹ��Ƥ�w�\��ȟ�����������ǻ�eҺ���������صȣ������ز��l�Y�İl���ʼs��2.2%����Ҫ�и�Ⱦ����������Ѫ����ǻ�ȳ�Ѫ���[���Nֲ���ι���˥�ߡ��c���ȡ�����gǰ�ʂ䡢�������Ҏ�����ʴ_��λ�͜p�����ڴΔ��ǽ��Ͳ��l�Y�l���ʵ���Ҫ������
�������l�Y�ķN�
�������ں�C���� ��Ҫ���F��l�ᡢ��ʹ�ȣ���Ҋ����Ѫ����ȣ����wԭ������̎����Ҫ���g��ӏ��O�o��ݔҺ��ֹʹ�����Y̎�������ڙz�y���I���ܡ�
������Ⱦ ��Ҫ�и�ē�[�������c��Ⱦ�ȡ��A����ʩ��������o���������g���ÿ������A����Ⱦ��
������������Ѫ ��Ҫԭ����ʳ���¶��o�}������Ѫ���ߑ����ԝ�����Ѫ���A�����ί����������Ї����T�}�߉��Ļ��ߣ��gǰ����̎���T�}�߉����g��Ҏʹ�����ᄩ���A�������ԝ�����Ѫ����Ѫ���ί������z�y�����w������ʳ���e�O�U�ݡ�ݔҺ��ֹѪ��ݔѪ�����ᡢ�����ȣ���Ҫ�r�Ѓ��R��ֹѪ��
������ǻ�ȳ�Ѫ �R�����Fȡ�Q�ڳ�Ѫ����������Ѫ�o���@�Y���Ѫ����r�����и�Û����ʹ�����ؕr���亹��Ѫ���½����ݿ˰Y�ԭ����Ҫ���[���^���\�����̺��[�����ѣ���������Ѫ���ܲ���K�����c��Ѫ���A����ʩ�������������m���C������Ӳ����Ѫ���ܲ�Ļ��ߣ��мm�������ί������ڱ�\�����ò��ø�ǻ�R�»����_��ֱҕ���M�У���Ƥ���l�ί��r���M���p�ٴ��̴Δ���ᘵ����ڽY�������ٴγ�����CT ���裬�ų��Пo�[�����ѡ���Ѫ�ȱ��F���ί������z�y�����w�����e�O�U�ݡ�ݔҺ��ֹѪ��ݔѪ�������ȣ���Ҫ�r�����g̽��ֹѪ��
�����[���Nֲ �[���Nֲ��Ҫ�����ڷ��Ͷ�δ�����ɡ��A����ʩ�������̑��ʴ_��λ�����ⷴ�Ͷ�δ��̣�����M��^�����ֱ�ӌ�늘O��˻أ����Ǒ�ԓ��ԭλ���ں���������¶�λ��
�����ι���˥�� �ι���˥�ߵ���Ҫԭ�����ί�ǰ��Ӳ���̶��أ����߸ι��ܲ���߰l�����ز��l�Y�����Ⱦ����Ѫ�ȣ����A�����ί���ʩ�������������m���C���ι���Child-Pugh C����������ˮ�������S��Ⱦ�������C���g��ע���A���������l�Y�İl�����A����Ⱦ���зe�O�o���ί���
���������K���p�� �[������đ�ҡ�θ�c��đ�ܡ������Ȼ�λ�ڵ�һ���T�^���ΰ�Ĥ�µȲ�λ�r���M�н�Ƥ����·���������ί����ן�p�������K�����}�ܡ������@Щ��λ���[������ԓ�M���ܲ��ø�ǻ�R�»����_�����gֱҕ�����l�����ί������������K���M�и��x���o��
�����u�r���S�L
�����ί���1 ���Ͳ������CT/MRI�����߳���Ӱ�����u�r���گ�Ч��
������ȫ���ڣ�Complete Response��CR��
�������K����CT/MRI ���߳���Ӱ�S�L�@ʾ���[�����څ^�����ܶȣ������F����������}��δҊ������
��������ȫ���ڣ�Incomplete Response��ICR��
�������K����CT/MRI ���߳���Ӱ�S�L�@ʾ���[������Ⱦֲ����}���Џ�������ʾ���[��������
�������⣬���ί������[�������ߣ������M���ٴ������ί�����ɴ����ں������[���������t�_���������ί�ʧ������ԓ�x�������ί��ֶΡ�
�����S�L
�����g��ǰ2����ÿ�Ͳ������CT/MRI���߳���Ӱ���Լ��ι��ܡ��[����־��ȣ��^�첡�������r���[����־���׃����֮��ÿ2��3���Ͳ��[����־�����Ӱ���߸�����CT/MRI�� ����Ӱ��CT/MRI�g���M�У��������ÿ3��6���Ͳ��[����־��ʳ���Ӱ���߸�����CT/MRI������Ӱ��CT/MRI�g���M�У��������S�L�Y���Д��[���Ͱl���Mչ��r���¡�
�����ֲ��[���Mչ��local tumor progression��
�����[����ȫ���ں����������߅�����F�µIJ���²����c���������B��
�����²��new lesion��
�������������l���IJ��
����
�����������l����ᘵĹ�����B
�����h̎�D�ƣ�distant recurrence��
�������F������D���
��������
�������L�U��λ�[�������l�����[������đ�ҡ�θ�c��đ�ܡ������Ȼ�λ�ڵ�һ���T�^���ΰ�Ĥ�µȲ�λ������Σ�U��λ�����@Щ��λ���[���M�����l�����ί������ڟ�p�������K�����}�ܡ��[�����ѡ���Ѫ���L�U�����Ҫ�eС�ġ�
�������ڸ��L�U��λ���[������ԓ�M���ܲ��ø�ǻ�R�»����_�����gֱҕ���M�������ί����Ա㌦�������K���M�и��x���o��Ҳ�Ј�����˹���ˮ���˹���ˮ������������ַ��������������������l�����ί��Ĉ����
�����M����ˣ��īI������l�����ί�Σ�U��λ�[���į�Ч�c������λ�[����ț]���@�����
�����������l����
����Ŀǰ���õ����l�����ί��xһ�������܉��_�������ڷ���һ���3.0��5.0 cm�����Ԍ��ڣ�5.0 cm���[�������c���l�ί��^�y�_����ȫ���ڡ��īI��������ö����w��ģ�Ͷ�ᘶ��c�ί���ΰ��IJ�ᘷ����M�з��Ͷ�����ڣ�����ʹ���ڷ����_��7.0 cm���ϡ�
�������l������������
�������īI��������l�����ϸ΄��}˨��������TACE����PEI�ȣ�������߯�Ч���e�nj����[����3 cm���߶����[�������ί�����������x�������l�����ί�ʧ���ߣ����x�������ί���ʽ�������g�г���TACE�����Ӱ���ˎ�������������ȣ�����l�h̎�D���ߣ������]�ϑ�����Ч��ȫ����ˎ���ί���
�������c�����R���ƶ����ң����ϳ�������ࡢ�~���������Ρ������ӡ����÷�����ɽ������A�������¡��R�����������B����ġ��X��܊���R���������������O�ı����uӢ�A���������S־�¡��n��κ�����衢�˺�㑡��Y�찲����Ƽ������������ҫ܊
TAG�� �ΰ� �ֲ����� �ί�
���PˎƷ
�[���ƌ���
�������P����
-
�������d��...
����T����
-
�������d��...
��������
-
�������d��...
���TˎƷ
- �༪��
- ����ɳ
- ���_�P
- ���S͡
- �漪�W
- �ͷ��f�����z��
- �ͷ��t��ɼ�z��
- �������z��
- ʳ��ƽɢ
- ��һ�z��
- �������z��
- ����ƽ��
- �ͷ������z��
- ���ɢ�Y��
- ��κ��Ʀ��
- ���Y�����ڷ�Һ
- �����z��
- �Ώ͘�Ƭ
- ־���z��
- �fđ���Ϳڷ���Һ
- �庣�`����
- �J�S�z��
- �S���_
- ��Ī��
- ���w��
- ������
- ������
- ������̹
- ���Y����Ƭ
- ������
- ������˾
�[����ˎƷ
- ˎƷ���}������
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- ���oӛ�
- ���oӛ�
- ���oӛ�
- ���oӛ�
�������- ��Ҋ���} | ����ָ�� | ˎ�W���� | ���Ҋ | �Ͷ�V | ���Ʒ��� | ���t��ˎ | ˎ������
���Ʒ����- �[���� | �β��� | �� | ����� | Ƥ�w�Բ��� | �� �� | �L�����߿� | ��Ѫ�ܿ� | ���� | ��������ˎ
ˎƷ��ُ����- �[����ˎƷ | �����ˎƷ | �β���ˎƷ | �ۿ�ˎƷ |Ƥ�w�Բ���ˎƷ | ��ˎƷ | �L�����߿�ˎƷ
ˎ���Y�|- ��I���ˠI�I���� | ˎƷ���I�S���C | ˎƷ���I�|������Ҏ���J�C | ʳƷ�l���S���C | ���WˎƷ��Ϣ�����Y���C
���WˎƷ��Ϣ�����Y���C����̖��(��)-�ǽ��I��-2006-0015 ��ICP�䰸̖: ��ICP��09020315̖
�͑����՟ᾀ��400-101-6868 Ͷ�V�c���h��020-66843700
����˾���귨����� �V�|����ʢ�_�Ɏ�����
����˾���͑��ĺϷ�������ܷ��ɱ��o�� �κ��ַ�����˾���͑�������κΆ�λ�͂��˱،��ܵ����ɵ��� ��








